Cómo sabemos, los hábitos de una mujer embarazada afectan la salud de su hijo, sin embargo el impacto que esto puede tener en la salud de las siguientes generaciones resulta sorprendente. Estudios sobre eventos trágicos en la historia de la humanidad, como la hambruna de Holanda, han esclarecido la relación entre la nutrición y las características heredadas a los hijos. Asimismo, existen registros históricos y médicos que vinculan la nutrición de los abuelos con la esperanza de vida y salud de los nietos. La forma de explicar este fenómeno es mediante la epigenética, una rama de la biología que toma en cuenta los factores ambientales en el desarrollo de un organismo.
La hambruna de invierno en el oeste de Holanda inició en diciembre de 1944, meses antes de que finalizara la Segunda Guerra Mundial. El suministro de comida en las regiones ocupadas por los alemanes llegó a ser muy limitada debido al bloqueo de trasporte terrestre de bienes entre Amsterdam y otras ciudades cercanas. A la vez, el clima fue muy severo y los campos agrícolas estaban arruinados por la guerra. Las raciones de alimento por día fueron inferiores a 500 calorías, menos de una cuarta parte recomendada para su consumo, hasta la liberación de la ciudad en mayo de 1945 (fig.1). Para esa fecha 18 mil personas murieron de hambre [1]
 Fig. 1 Niños esperan a ser alimentados durante la hambruna de invierno en Holanda. Tomado de Ahmed, 2010
Fig. 1 Niños esperan a ser alimentados durante la hambruna de invierno en Holanda. Tomado de Ahmed, 2010
Este acontecimiento posee gran relevancia ya que es usado como un ejemplo por varios investigadores para identificar el efecto de la desnutrición prenatal en humanos. Se caracteriza, además, porque la hambruna fue impuesta en una población previamente bien alimentada, delimitando, así, el inicio de la desnutrición en la población.
Los niños concebidos durante esta hambruna fueron más pequeños, con bajo peso y con problemas de salud que perduraron hasta su vida adulta, comparados con sus hermanos procreados antes o después de la hambruna [2]. Por supuesto, estás características son congruentes con la alimentación que llevó su madre y no son para sorprenderse. Lo que sí resulta asombroso es que cuando estos niños crecieron, aún cuando la guerra había ya terminado y mejoraron su alimentación, a su vez procrearon niños de menor talla. Entre los efectos que se asocian a la exposición prenatal de la hambruna en Holanda están: bajo peso al nacer, diabetes, obesidad, enfermedades coronarias y al menos un grupo de esas personas analizadas también tuvieron hijos más pequeños [3].
Este hecho es muy importante, porque sugiere que la dieta de una mujer embarazada afectará la salud, no sólo de su hijo, si no también sería heredada a su nieto y a posibles generaciones futuras.
Otro caso semejante se reporta en la hambruna de Biafran en Nigeria (1968-1970). Los niños procreados en esa época fueron propensos a desarrollar hipertensión, obesidad y diabetes tipo 2 [4]. Es posible que este periodo de restricción de nutrientes durante la gestación fomente al feto a ahorrar energía durante su vida, lo que se convierte en un problema cuando las calorías suministradas ya no son escasas y los niños tienen la disponibilidad adecuada de alimento, lo que puede desencadenar en obesidad.
Por otro lado, en la Gran Hambruna China (1958-1961), causada por la mala administración de su líder Mao Zedong y al severo clima, la exposición prenatal a este periodo de escases de alimento incrementó el riesgo de esquizofrenia en los niños [1].
A todo lo anterior, ¿cuál es el mecanismo que permite que eventos extremos en la nutrición de la madre afecten no sólo a sus hijos sino también a las siguientes generaciones? ¿Se trata de un tipo de marca en la información genética de los individuos que le permite recordar a su progenie las situaciones ambientales en las que se desarrollaron? ¿Sólo la alimentación de la vía materna se ve involucrada? La respuesta a estas preguntas se encuentra en el estudio de la epigenética.
¿Qué es la epigenética?
Un punto de vista convencional de la evolución es que nuestro DNA transporta toda nuestra información heredable. Esta información está presente en el óvulo de nuestra madre y en el espermatozoide del padre, que fusionados forman a un individuo. Creemos que cuando nacemos está información está fija y la pasaremos sin alteración a nuestros hijos. Sin embargo en años recientes, surge una nueva concepción respecto a la influencia de varios factores que afectan a los genes que se heredan. A lo largo de nuestra existencia estamos expuestos a distintos factores ambientales como: la radiación solar, distintos químicos, el estrés e incluso el tipo de alimentación que modifican la información que se transmitirá a nuestros descendientes por generaciones, en forma de “etiquetas” en el DNA. Esta información transmitida funciona como un “recordatorio” para los hijos sobre la exposición ambiental a la que se sometieron los padres. Este es uno de los fundamentos de la epigenética (del griego epi, en o sobre y genética, más allá de la genética).
La epigenética se refiere, entonces, a cambios en la expresión genética, es decir que esté activo o no un gen, sin que se involucren cambios en la secuencia de DNA (genotipo). Es, en otras palabras, los cambios que ocurren en las características o rasgos observables de un organismo (fenotipo) sin cambiar el genotipo [5].
Los cambios epigenéticos ocurren normalmente en el cuerpo y se manifiestan en la diferenciación de las células en todas las variantes que existen: células de la piel, del cerebro, del hígado etc. Todas estas células poseen la misma información genética, tan es así que se podría clonar un organismo a partir de cualquier célula somática de nuestro cuerpo, sin embargo al final la función de cada tipo celular es muy distinta.
Una manera sencilla de ejemplificar los cambios epigenéticos es con las investigaciones realizadas en gemelos monocigóticos considerados genéticamente idénticos. Estos estudios se realizan para evaluar el efecto del ambiente en el desarrollo de ciertas enfermedades y como la epigenética puede hacer la diferencia en cuanto a los cambios que se producen en el fenotipo de los gemelos [6]. Al inicio, ambos bebés comparten el mismo ambiente en el que se desarrollan, por tanto están sometidos a las mismas condiciones. Sin embargo cuando los gemelos crecen, cambian las condiciones a las que están sometidos: contaminación, tipo de alimentación, el hábito de fumar, actividad física, etc. Por esta razón, aunque los gemelos tenga la misma información genética, puede ser que uno de los dos desarrolle alguna enfermedad como cáncer o diabetes y el otro no.
La forma en la que se podría explicar la epigenética es imaginarnos que toda la información genética de un individuo son las letras de un libro. Por si solas estas letras no tienen coherencia, lo que le da sentido a estas letras son: los espacios, los signos de puntuación, de interrogación, exclamación etc., que corresponden a la epigenética. Las letras representarían nuestro DNA que contiene todas las instrucciones necesarias para construir las partes de nuestro cuerpo. Una de las peculiaridades del DNA es que mide aproximadamente dos metros de manera lineal y para poder ingresar a una célula diminuta, se debe súperenrollar y esto lo logra gracias a unas proteínas llamadas histonas que funcionan como carretes (fig.2).
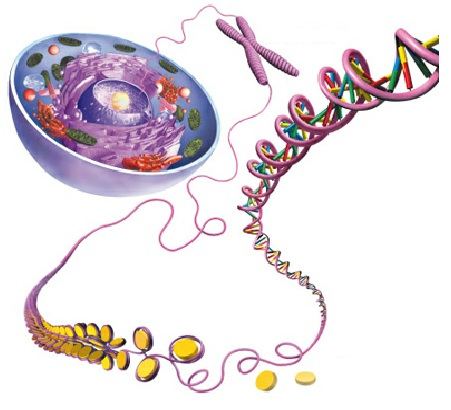
Fig. 2. Forma en la que el DNA se enrolla alrededor de las histonas (círculos amarillos) para poder entrar a la célula. El último nivel de compactación es el cromosoma. Tomado de: http://explosion-del-saber-para-entretener.blogspot.mx/2012/06/adn-posee-cuatro-estructuras.html
Por otra parte, algunos de los cambios que le dan sentido a nuestra información genética, que en el ejemplo descrito anterior corresponden a los signos de puntuación, son sustancias químicas que se unen a las histonas o al propio DNA. Uno de estos químicos es el grupo metilo, un compuesto formado por un átomo de carbono y tres de hidrógeno, que puede obtenerse de la dieta en nutrientes como el ácido fólico o las vitaminas B. Estos grupos metilo funcionan como etiquetas que se acumulan durante nuestro desarrollo embrionario y a lo largo de nuestra vida alterando nuestra expresión génica y que, incluso, pueden heredarse [7]. Cuando se unen grupos metilo a las histonas provocan que se compacte el DNA, este proceso se denomina metilación y ayuda, comúnmente, a silenciar un gen, es decir a que una proteína en específico no se produzca o se produzca en menor proporción (fig.3). La metilación también se lleva a cabo directamente en el DNA, permitiendo que se apague la función de un gen y, por tanto, la producción de alguna proteína.
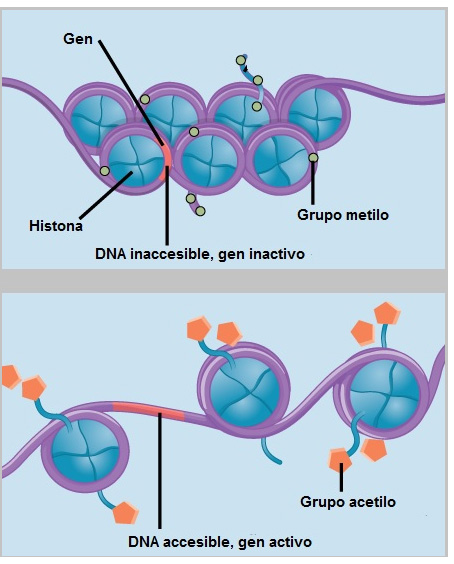
Fig. 3 La imagen de arriba indica como los grupos metilo compactan el DNA alrededor de las histonas provocando que los genes sean inactivos. El panel de abajo, muestra lo contrario, un grupo de compuestos llamados acetilo provocan que el DNA esté más holgado, induciendo su accesibilidad para la subsecuente producción de una proteína.
Modificado de http://commonfund.nih.gov/epigenomics/figure
Estudios en ratones han demostrado lo importante que es la dieta de la madre en la epigenética de su descendencia. Todos los mamíferos tenemos un gen llamado agouti, cuando este gen no tiene grupos metilo (desmetilado), provoca en los ratones que su pelaje sea amarillo, sean obesos y propensos a diabetes y cáncer. Cuando el gen está metilado (así se debe de presentar en un ratón normal), los ratones son de color café y tienen un menor riesgo de presentar estas enfermedades (fig.4). Ambos ratones son genéticamente iguales, sólo difieren en esa marca en su DNA, o sea en la presencia del grupo metilo. Para prevenir estos problemas de salud, la dieta de la madre tiene que ser rica en grupos metilo, que se obtienen del folato o la colina [7].

Fig. 4. El ratón de la izquierda posee el gen auguti desmetilado lo que provoca que el color de su pelaje sea amarillo además de presentar diversas enfermedades. Con un cambio en la dieta, incrementando los niveles de ácido fólico y colina, este ratón puede procrear un ratón sano (derecha), se observa claramente el cambio en el color de su pelaje. Tomado de http://discovermagazine.com/2006/nov/cover
Regresando al ejemplo de los niños concebidos durante la hambruna en Holanda, un grupo de investigación de la Universidad de Columbia examinaron el DNA de 60 de estos individuos, seis décadas después de su nacimiento. Compararon a las personas que fueron expuestos a la hambruna durante los primeros meses de su desarrollo embrionario con sus hermanos del mismo sexo. Los científicos analizaron específicamente el gen del factor de crecimiento insulinínico tipo II (IGF2) que se encarga de formar una hormona de crecimiento esencial durante la gestación. Encontraron que este gen presentaba un bajo promedio de metilación en los niños de la hambruna comparado con el gen IGF2 de sus hermanos. Al disminuir la metilación, está hormona se expresaría más. Aunque está característica no se ha asociado al peso corporal, es posible que este asociado a enfermedades como diabetes y ciertos cánceres [3].
También afecta lo que come papá
Hay que recalcar que no sólo las dietas extremas afectan la salud de los hijos, sino que ciertas sustancias son esenciales durante la gestación. El ácido fólico, por ejemplo, previene la malformación de los bebés, por esa razón es recetado por los médicos a las mujeres embarazadas. Un hecho curioso es que no sólo es importante que la madre ingiera ácido fólico, sino que estudios científicos sugieren que la dieta de los padres también puede influir en la salud de los hijos. La forma en la que se transmite esta información es a través del espermatozoide.
En una investigación llevada a cabo en ratones machos se comparó el efecto del ácido fólico suministrado en dos tipos de dietas: una rica en folatos y una deficiente en estos. La descendencia de los machos con la dieta deficiente en folatos presentó defectos de nacimiento como malformaciones del cráneo y del músculo esquelético, caso contrario con la descendencia del macho con la dieta rica en esté nutriente. Aunque el estudio fue realizado en ratones, puede extrapolarse a los seres humanos [8].
Otro caso muy interesante es un estudio que asocia la alimentación de abuelos paternos con la expectativa de vida de sus nietos en la comunidad de Överkalix en Suecia. Esta comunidad se caracteriza por poseer un registro detallado de los nacimientos, defunciones y condiciones de vida de los habitantes. La investigación se basó en el seguimiento de personas nacidas en 1905 que fueron clasificadas por la disponibilidad de comida de sus padres y abuelos (mediante datos históricos sobre cosechas y precio de alimentos). Interesantemente se encontró que la cantidad de comida que ingería el abuelo paterno a la edad de 9-12 años, afectaba la esperanza de vida de sus nietos: la escasez de comida estaba relacionada a una esperanza de vida mayor, caso contrario, una dieta abundante se asociaba a una esperanza de vida corta. En el caso de que el abuelo experimentara una disponibilidad moderada de comida durante su infancia no observaron algún cambio en la supervivencia de sus nietos [9].
Contexto nacional
En nuestro país, los estudios epigenéticos en la población son escasos, un ejemplo es el realizado en Tercera Chica San Luis Potosí, sobre la exposición de toxinas producidas por la fabricación informal de ladrillo que han sido asociadas a cáncer y daño de órganos [10].
Asimismo, algunos investigadores que se dedican al estudio de la epigenética son: El Dr. Félix Recillas Targa, investigador del Departamento de Genética Molecular del Instituto de Fisiología de la UNAM, que se dedica a comprender los mecanismos epigenéticos en cáncer y otros padecimientos como la talasemia. El Dr. Raúl Álvarez Venegas del Laboratorio de Cromatina y Epigenética del CINVESTAV Irapuato, que se enfoca a la regulación epigenética en plantas y su respuesta a patógenos. La Dra. Gertrud Lund del Laboratorio de Epigenética, también del CINVESTAV Irapuato, que estudia la metilación del DNA en el desarrollo de la semilla de maíz y de la aterosclerosis. La Dra. Vilma Araceli Maldonado Lagunas del INMEGEN se enfoca a la epigenética del cáncer de mamá, de diabetes y obesidad, entre otros.
Conclusiones
Hemos dado un breve bosquejo de como el ambiente, específicamente la alimentación, afecta el desarrollo de los individuos y que, además, esta influencia ambiental puede heredarse a las siguientes generaciones debido a marcas epigenéticas en su información genética. Ahora podemos comprender el dicho que dicta: somos lo que comieron nuestros padres y abuelos.
Fuentes de consulta
[1] Ahmed F. “Tales of adversity”. Nature, vol. 468, pp S20, Dec. 2010
[2] Lumey L. 1992. “Decreased birthweights in infants after maternal in utero exposure to the Dutch famine of 1944-1945”. Paediatric Perinatal Epidemiology 6(2):240-53.
[3] Heijimans B., Tobi E., Stein A., Putter H., Blauw G., Susser E., Slagboom E., and Lumey L. 2008. “Persistent epigenetic differences associated with prenatal exposure to famine in humans”. PNAS, vol 105 pp. 17046–17049, September 2008.
[4] Roseboom T., Painter R., Van Abeelen A., Veenendaal M and de Rooij S. Review “Hungry in the womb: What are the consequences? Lessons from the Dutch famine” Maturitas, vol. 70, pp. 141– 145, June 2011.
[5] Epigenetics: Fundamentals. Disponible en: http://www.whatisepigenetics.com/fundamentals/
[18 de diciembre de 2014]
[6] Fraga M. Ballestar E., Paz M., Ropero S., Setien F., Ballestar M., Heine-Sunñer D., Cigudosa J., Urioste M., Benitez J., Boix-Chornet M., Sanchez A. Ling C., Carlsson E., Poulsen P., Vaag A., Stephan Z., Spector T., Wu Y., Plass C and Esteller M. “Epigenetic differences arise during the lifetime of monozygotic twins”. PNAS, vol. 102, pp. 10604–10609, July 2008.
[7] Nutrition and the Epigenome. Genetic Science Learning Center. Learn.Genetics. Disponible en: http://learn.genetics.utah.edu/content/epigenetics/nutrition/
[7 de diciembre de 2014]
[8] Lambrot R, Xu C., Saint-Phar S., Chountalos G., Cohen T., Paquet M., Suderman M., Hallett M., and Kimmins S. “Low paternal dietary folate alters the mouse sperm epigenome and is associated with negative pregnancy outcomes”. Nature Communications, vol. 4, pp. 1-13, Dec 2013.
[9] Bygren L., Kaati G. and Edvinsson S. “Longevity determined by paternal ancestors’ nutrition during their slow growth period”. Acta Biotheoretica, vol. 49, pp. 53-59, Nov 2001.
[10] Alegría J., Barretta F., Batres L., Carrizales L., Pérez I., Baccarelli A. and Bertazzi P. “Epigenetic markers of exposure to polycyclic aromatic hydrocarbons in Mexican brickmakers: A pilot study.” Chemosphere, vol. 91, pp. 475-480, Jan 2013.
Glosario
DNA. Ácido desoxirribonucleico, molécula dentro de la célula que transporta la información genética que pasa de una generación a otra.
Célula somática. Todas las células del cuerpo, excepto las células reproductivas: el espermatozoide y el óvulo.
Colina. Nutriente esencial agrupado con las vitaminas del grupo B
Gen. Unidad básica de la herencia pasada de padres a hijos. Los genes son segmentos de DNA. Muchos genes contienen la información para formar una proteína específica.

Que alegría observar que espacios como este se dediquen a la divulgación de temas científicos con lenguaje digerible, para hacerla accesible a las personas que no están familiarizadas con estos temas. Felicidades a ustedes y a la Dra. López Ruiz.
Me gustaLe gusta a 1 persona
Hola Miguel, muchísimas gracias por parte de todo el equipo. Lo hacemos con la mejor intención. Indudablemente, la Dra. López Ruiz tiene un gran talento para hacer fácil lo difícil. De tu parte le enviaremos tus felicitaciones ¡Un abrazo!
Me gustaMe gusta
Enhorabuena!!, excelente información. Gracias. Saludos desde España.
Me gustaLe gusta a 1 persona
Muchas gracias Ricardo por tu comentario y por leernos. ¡¡Saludos!!
Me gustaMe gusta